从干细胞到器官再生 日本人与动物嵌合胚胎试验的技术路径与伦理边界
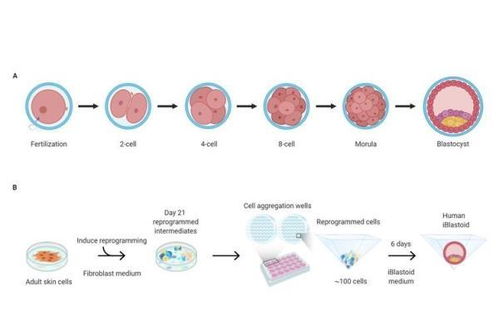
日本在人与动物嵌合胚胎研究领域取得了一系列突破性进展,其核心目标是通过将人类干细胞植入动物胚胎,培育出可供移植的人类器官。这项前沿科技不仅涉及复杂的生物学技术,更触及深刻的伦理边界。本文将解析其背后的关键技术——特别是胚胎如何形成,以及人体干细胞在其中扮演的角色。
一、技术核心:嵌合胚胎的构建
日本研究团队采用的主要方法是“囊胚互补法”。该过程并非传统的“受精”概念,而是通过基因编辑与干细胞移植实现的。
- 动物胚胎准备:研究人员首先利用基因编辑技术(如CRISPR-Cas9)敲除猪或大鼠等动物胚胎中形成特定器官(如胰腺)的关键基因,使其自身无法发育出该器官,从而为人类细胞的“入驻”腾出生态位。
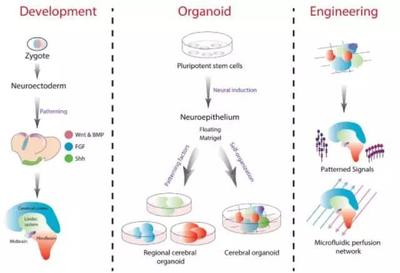
- 人类干细胞注入:将人类诱导多能干细胞(iPS细胞)注入经过编辑的动物早期胚胎(囊胚期)中。这些iPS细胞并非来自精卵结合,而是通过将成年人体的皮肤细胞等体细胞进行“重编程”获得,具备分化成任何类型细胞的潜力。
- 嵌合体发育:胚胎被植入代孕动物子宫。在理想情况下,人类iPS细胞会“填补”动物胚胎缺失的器官发育路径,最终在动物体内形成一个由人类细胞主导的、功能正常的器官(如肾脏或胰腺)。这个器官在遗传上主要属于人类,可用于移植研究,理论上能极大缓解器官短缺问题。
二、基石:人体干细胞技术的核心作用
整个研究的基石是人体干细胞技术,尤其是iPS细胞技术。
- 来源与优势:iPS细胞避免了使用人类胚胎的伦理争议,可从患者自身细胞获得,理论上能实现“个性化器官”培育,移植后排异风险极低。
- 应用挑战:在嵌合胚胎中,如何精确控制人类干细胞的分化方向,确保其只发育成目标器官而非扩散到动物大脑或生殖系统,是技术上的重大挑战。日本的规定严格限制此类胚胎发育超过14天(囊胚期),且禁止将其移植到人类子宫,正是为了防止不可控的伦理风险。
三、伦理与监管:谨慎前行
日本是全球首个为人与动物嵌合胚胎研究制定明确国家指南的国家。其核心原则是:
- 研究仅限于器官再生,严禁涉及生殖细胞(精卵)的嵌合。
- 严格监控人类细胞在动物大脑中的占比,防止产生具有人类认知特征的生物。
- 所有研究需经国家层面严格的伦理审查。
###
日本的人与动物嵌合胚胎研究,代表了再生医学领域一项大胆的探索。它通过创新的“囊胚互补法”结合先进的iPS细胞技术,绕开了传统受精过程,旨在制造可供移植的人类器官。这项技术犹如行走在伦理的钢丝上,其未来发展不仅取决于技术的精进,更依赖于全社会在科学伦理上达成的共识与建立的牢固护栏。科学与伦理的平衡,将决定这项技术最终是为人类健康带来福音,还是打开潘多拉魔盒。
如若转载,请注明出处:http://www.fadien.com/product/44.html
更新时间:2026-05-30 00:20:01