肝脏与肠道酯酶在药物代谢中的关键角色及其与新药研发及干细胞技术的协同展望
在生物医药领域,药物在体内的代谢过程是新药研发与精准医疗的核心议题。其中,肝脏和肠道作为关键的代谢场所,其富含的酯酶在药物转化中扮演着不可或缺的角色。与此人体干细胞技术的飞速发展为药物代谢研究及新药开发提供了前所未有的工具与视角。本文将探讨肝脏和肠道酯酶在药物代谢中的作用机制,并阐述其与新药研发及干细胞技术应用的紧密联系。
一、 肝脏与肠道酯酶:药物代谢的前沿哨兵
酯酶是一类能够水解酯键的水解酶,广泛分布于人体各组织,尤其在肝脏和肠道中活性极高。它们是药物I相代谢(官能团化反应)的重要参与者。
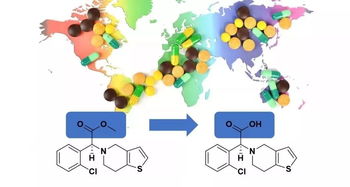
- 肝脏酯酶的核心地位:肝脏是药物代谢的“主要化工厂”。肝细胞富含多种酯酶,如羧酸酯酶、胆碱酯酶等。许多口服药物(尤其是前药,即本身无活性或活性较低,需在体内代谢转化后才发挥药效的化合物)经肠道吸收后,通过门静脉首先进入肝脏。肝脏酯酶能迅速水解这些药物的酯键,将其转化为活性形式,或为进一步的II相代谢(结合反应)做准备。这一“首过效应”直接决定了药物的生物利用度和疗效强度。例如,抗病毒药物奥司他韦(达菲)就是典型的前药,需经肝脏酯酶转化为活性代谢物才能发挥抗流感病毒作用。
- 肠道酯酶的“守门人”作用:肠道不仅是吸收器官,其上皮细胞和肠道菌群也表达丰富的酯酶。药物在口服后,尚未进入全身循环之前,便会与肠道酯酶接触。肠道酯酶代谢可以导致部分药物在吸收前即被水解失活或激活,显著影响口服药物的生物利用度。肠道菌群来源的酯酶其代谢模式可能与宿主酶系不同,增加了药物反应的个体差异性和复杂性。
作用:肝脏和肠道酯酶共同构成了药物进入体循环前的双重代谢屏障与激活站点。它们影响着药物的起效速度、作用强度、持续时间以及潜在的毒副作用,是理解药物个体差异、设计合理给药方案的关键。
二、 酯酶研究在新药研发中的战略意义
对肝脏和肠道酯酶机制的深入理解,直接驱动着新药研发策略的创新。
- 前药设计:利用酯酶的特异性水解,科学家可以设计前药。这能改善原药的不良理化性质(如溶解性差、口服吸收率低)、提高靶向性、或掩盖不良味道。设计时需精确预测前药在肠道和肝脏中的代谢速率与路径,以确保其在正确的位置、以合适的速率释放活性成分。
- 规避不良代谢与药物相互作用:新药分子若含有易被酯酶水解的基团,需评估其代谢稳定性。不稳定的药物可能过早失活,或产生具有毒性的代谢产物。新药也可能抑制或诱导酯酶的活性,从而影响与其联用的其他药物的代谢,产生复杂的药物-药物相互作用。因此,在临床前研究中,利用人源肝微粒体、重组酯酶或肝细胞模型进行酯酶代谢稳定性及抑制/诱导潜能测试,已成为标准环节。
- 个体化用药的 biomarker:酯酶的活性与表达量存在基因多态性(如羧酸酯酶1 CES1基因变异),这导致不同人群对某些药物(如抗血小板药氯吡格雷的前药转化)的代谢能力差异巨大。在新药研发的临床阶段,对受试者进行相关酯酶基因型筛查,有助于解释疗效与安全性差异,并为未来的精准用药提供依据。
三、 人体干细胞技术的革命性赋能
传统研究多依赖动物模型或永生化细胞系,但这些模型与人体真实的生理和代谢环境存在差距。人体干细胞技术的出现,特别是诱导多能干细胞(iPSC)和类器官技术,为药物代谢研究带来了范式变革。
- 构建人源化代谢模型:iPSC技术可以将个体(包括健康人或特定疾病患者)的体细胞(如皮肤成纤维细胞)重编程为多能干细胞,进而定向分化为功能性的肝细胞样细胞或肠道上皮细胞。这些细胞能够表达包括酯酶在内的一系列药物代谢酶,且遗传背景与供体一致。这为研究酯酶活性个体差异、基因多态性对药物代谢的影响,提供了高度人源化、可定制的体外模型。
- 创建“肝脏-肠道”互作类器官系统:利用干细胞培育的肝类器官和肠类器官,能够更真实地模拟各自组织的复杂三维结构和功能。更进一步,科学家正在尝试将肝类器官与肠类器官在微流控芯片上共培养,构建“芯片上的肝-肠”模型。这种系统可以动态模拟口服药物经肠道吸收、代谢后,通过循环进入肝脏进行再代谢的完整过程,为研究酯酶在“肠-肝轴”上的级联代谢作用提供了前所未有的平台。
- 加速疾病建模与药物筛选:从特定遗传病或代谢性疾病患者衍生出的iPSC-肝/肠细胞,其酯酶功能可能天生异常。利用这些细胞模型,不仅可以深入研究疾病机制,还能高通量筛选针对该代谢环节的候选药物,评估新药在疾病背景下的代谢特征,实现“从实验室到临床”的精准衔接。
四、 未来展望:整合与精准
药物代谢研究将深度融合酯酶生物学、干细胞技术与人工智能。通过干细胞模型产生海量的个体特异性代谢数据,结合AI进行模拟预测,我们将能够:
- 更精准地预测新药在人群中的代谢命运与安全性。
- 设计更智能的前药,实现时空可控的靶向释放。
- 真正实现个体化用药,根据患者的酯酶基因型和干细胞模型测试结果,“量体裁衣”式地选择药物和剂量。
肝脏和肠道酯酶是调控药物体内旅程的关键分子开关。而人体干细胞技术,正为我们提供一套精准还原并操控这一过程的强大工具。二者的交叉融合,必将深刻推动新药研发从经验驱动向机理驱动、从“千人一药”向“千人千药”的范式转变,为攻克复杂疾病和实现精准医疗奠定坚实基础。
如若转载,请注明出处:http://www.fadien.com/product/56.html
更新时间:2026-06-03 21:53:23